Hai cốc có khối lượng bằng nhau đặt lên hai đĩa cân, cân thăng bằng. Cho 10,6 g NaHCO3 vào cốc bên trái và19,72g bột nhôm vào cốc bên phải. Nếu dùng dung dịch HCl 7,3% thì cần thêm vào cốc nào bao nhiêu gam để cân trở lại thăng bằng

Những câu hỏi liên quan
Trên hai đĩa cân đã thăng bằng, đặt hai cốc bằng nhau: Cho vào cốc bên trái 12 gam Mg; cho vào cốc bên phải 26,94 gam MgCO3, cân mất thăng bằng. Muốn cân trở lại thăng bằng như cũ phải thêm vào cốc Mg bao nhiêu gam dung dịch HCl 14,6% ? A. 16 gam. B. 14 gam. C. 15 gam. D. 17 gam.
Đọc tiếp
Trên hai đĩa cân đã thăng bằng, đặt hai cốc bằng nhau: Cho vào cốc bên trái 12 gam Mg; cho vào cốc bên phải 26,94 gam MgCO3, cân mất thăng bằng. Muốn cân trở lại thăng bằng như cũ phải thêm vào cốc Mg bao nhiêu gam dung dịch HCl 14,6% ?
A. 16 gam.
B. 14 gam.
C. 15 gam.
D. 17 gam.
Đặt hai cốc trên hai đĩa cân, rót dung dịch HCl vào hai cốc, khối lượng axit ở hai cốc bằng nhau. Hai đĩa cân ở vị trí thăng bằng. Thêm vào cốc thứ nhất một lá sắt, cốc thứ hai thêm vào một lá nhôm, khối lượng hai lá kim loại bằng nhau. Hãy cho biết vị trí của cân trong mỗi trường hợp sau:a. Hai lá kim loại tan hết.b. Thể tích H2 sinh ra ở mỗi cốc bằng nhau. (đo cùng điều kiện nhiệt độ và áp suất)
Đọc tiếp
Đặt hai cốc trên hai đĩa cân, rót dung dịch HCl vào hai cốc, khối lượng axit ở hai cốc bằng nhau. Hai đĩa cân ở vị trí thăng bằng. Thêm vào cốc thứ nhất một lá sắt, cốc thứ hai thêm vào một lá nhôm, khối lượng hai lá kim loại bằng nhau. Hãy cho biết vị trí của cân trong mỗi trường hợp sau:
a. Hai lá kim loại tan hết.
b. Thể tích H2 sinh ra ở mỗi cốc bằng nhau. (đo cùng điều kiện nhiệt độ và áp suất)
a) Giả sử mỗi lá kim loại nặng 1 (g)
- Xét cốc thứ nhất:
\(n_{Fe}=\dfrac{1}{56}\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
\(\dfrac{1}{56}\)------------------->\(\dfrac{1}{56}\)
=> \(m_{tăng}=1-\dfrac{1}{56}.2=\dfrac{27}{28}\left(g\right)\) (1)
- Xét cốc thứ hai
\(n_{Al}=\dfrac{1}{27}\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
\(\dfrac{1}{27}\)-------------------->\(\dfrac{1}{18}\)
=> \(m_{tăng}=1-\dfrac{1}{18}.2=\dfrac{8}{9}\left(g\right)\) (2)
(1)(2) => Khối lượng chất trong cốc thứ nhất tăng nhiều hơn so với khối lượng chất trong cốc thứ hai
=> Cân nghiêng về cốc thứ nhất
b)
Do thể tích khí H2 thoát ra là bằng nhau
=> Cân ở vị trí cân bằng
Đúng 2
Bình luận (0)
Đặt hai cốc có khối lượng bằng nhau lên cân, cân thăng bằng, cho 10,6g Na2CO3 vào Cốc A và 11,82g BaCO3 vào cốc B. Sau đó thêm tiếp 12g dung dịch H2SO4(98%) vào cốc A thì cân mất thăng bằng. Nếu thêm từ từ dung dịch HCl(14,6%) vào cốc B cho tới khi cân thăng bằng thì tốn bao nhiêu g dung dịch.( Giả sử HCl và H20 bay hơi không đáng kể).
Help meeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeee :(((
2,6g dung dịch
ez
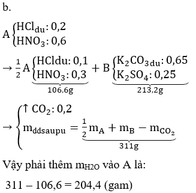
3-Cho 2 cốc A,B có cùng khối lượng. Đặt A, B lên hai đĩa cân, cân thăng bằng. Cho vào cốc A 126 gam K2CO3 và vào cốc B 85 gam AgNO3. Thêm vào cốc A 100g dung dịch H2SO4 19,6% và vào cốc B 100 gam dung dịch HCl 36,5%. Hỏi phải thêm bao nhiêu g H2O vào cốc A hay cốc B để cân lập lại thăng bằng
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.Giúp mình nha
Đọc tiếp
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
Giúp mình nha
\(n_{Fe}=\dfrac{7,84}{56}=0,14\left(mol\right);n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,14 0,14
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
'Mol: 0,3 0,45
⇒ Khối lượng đc thêm vào ở cốc A là 7,84-0,14.2=7,56 (g)
Khối lượng đc thêm vào ở cốc B là 8,1-0,45.2=7,2 (g)
⇒ Cốc A nặng hơn cốc B (do khối lượng axit được lấy vào 2 cốc bằng nhau )
Vậy cân ko còn ở vị trí thăng bằng
Đúng 0
Bình luận (0)
Đặt lên đĩa cân bên trái của cân Robecvan một quả cân 100g, rồi đổ cát khô lên đĩa cân bên phải cho đến khi cân thăng bằng.Bỏ quả cân 100g ra, đặt một cốc rỗng lên đĩa cân bên trái thì muốn 1 cân trở lại thăng bằng cân đặt thêm lên đĩa cân này 1 quả cân 50g, 1 quả cân 20g và 1 quả cân 5 g.A/Hãy xác định khối lượng của cốc.B/ Muốn đổ 40g bột ngọt từ túi vào cốc thì nên làm thế nào?
Đọc tiếp
Đặt lên đĩa cân bên trái của cân Robecvan một quả cân 100g, rồi đổ cát khô lên đĩa cân bên phải cho đến khi cân thăng bằng.
Bỏ quả cân 100g ra, đặt một cốc rỗng lên đĩa cân bên trái thì muốn 1 cân trở lại thăng bằng cân đặt thêm lên đĩa cân này 1 quả cân 50g, 1 quả cân 20g và 1 quả cân 5 g.
A/Hãy xác định khối lượng của cốc.
B/ Muốn đổ 40g bột ngọt từ túi vào cốc thì nên làm thế nào?
a) Tổng khối lượng của 3 quả cân là :
50+20+5=75(g)
Ta thấy cát khô có khối lượng 100g
Mà khối lượng của cốc + 75g=100g
=> Khối lượng của cốc là :25g
Đúng 0
Bình luận (0)
Người ta tiến hành thí nghiệm sau:- Đặt lên 2 đĩa cân (cân Robecvan): Đĩa cân A: cốc đựng dung dịch HCl; đĩa cân B: cốc đựng dung dịch H2SO4 loãng. Cân ở vị trí thăng bằng.- Thêm vào cốc A một dây Mg có khối lượng 3,6g; thêm vào cốc B lá nhôm có khối lượng 5,4g. Để cho toàn bộ kim loại tan hết.1) Viết PTHH của các phản ứng xảy ra?2) So sánh thể tích khí thoát ra ở 2 cốc?3) Xác định trạng thái của cân sau thí nghiệm? Cần phải thêm nước vào cốc nào? Bao nhiêu gam nước để cân trở lại vị trí thăng b...
Đọc tiếp
Người ta tiến hành thí nghiệm sau:
- Đặt lên 2 đĩa cân (cân Robecvan): Đĩa cân A: cốc đựng dung dịch HCl; đĩa cân B: cốc đựng dung dịch H2SO4 loãng. Cân ở vị trí thăng bằng.
- Thêm vào cốc A một dây Mg có khối lượng 3,6g; thêm vào cốc B lá nhôm có khối lượng 5,4g. Để cho toàn bộ kim loại tan hết.
1) Viết PTHH của các phản ứng xảy ra?
2) So sánh thể tích khí thoát ra ở 2 cốc?
3) Xác định trạng thái của cân sau thí nghiệm? Cần phải thêm nước vào cốc nào? Bao nhiêu gam nước để cân trở lại vị trí thăng bằng?
nMg=3,6/24=0,15 mol ; nAl=5,4/27=0,2 mol
1) Mg + 2HCl --> MgCl2 + H2 (1)
0,15 0,15 0,15 mol
2Al+ 3H2SO4 --> Al2(SO4)3 + 3H2 (2)
0,2 0,1 0,3 mol
b)(1) => vH2=0,15x22,4=3,36 l
(2) => V H2= 0,3x22,4=6,72 l
=> VH2(2) > VH2(1)
c) đặt dd HCl là A => dd H2SO4 = A
(1) => m dd sau = 0,15*24 + A -0,15 *2 =3,3 + A
(2) => m dd sau= 0,2*27 + A - 0,2 *2=4,8+A
=> cần thêm nước vào cốc thứ nhất và thêm số gam là
4,8 + A - (3,3 + A) = 1,5 g nước
Đúng 0
Bình luận (0)
Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Cho vào cốc A 102 gam chất a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi các phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để cân trở lại thăng bằng? b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch có trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?
Đọc tiếp
Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Cho vào cốc A 102 gam chất
a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi các phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để cân trở lại thăng bằng?
b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch có trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?
a.
|
|
AgNO3 |
K2CO3 |
| Ban đầu |
0,6 mol; 102 gam |
0,9 mol; 124,2 gam |
| Thêm vào |
→ HCl : 0 , 1 mol ↓ AgCl : 0 , 6 mol |
← H 2 SO 4 : 0 , 25 ↑ CO 2 : 0 , 25 |
| Sau phản ứng |
115,9gam |
213,2 gam |
| Thêm nước |
213,2 – 115,9 = 97,3 gam |
|
Đúng 0
Bình luận (0)
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
Đọc tiếp
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
HYJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJ



















